Professor Associado, Universidade Fernando Pessoa
| Outras vias metabólicas: | |||
| Química Orgânica: |
Os electrões libertados pela oxidação de substratos são transferidos pelas enzimas para moléculas especiais: os aceitadores de electrões. Os aceitadores de electrões podem ser de vários tipos, e os mais comuns são o NAD+ e o FAD. Cada uma destas moléculas pode receber dois electrões, transformando-se respectivamente em NADH+H+ e FADH2. Como as quantidades de NAD+ e FAD na célula são muito pequenas, é necessário haver mecanismos para transformar o NADH+H+ e FADH2 de novo em NAD+ e o FAD. Isto é feito por transferência dos electrões do NADH+H+ e FADH2 para outras moléculas, o que pode ocorrer por fermentação ou respiração. A distinção entre estes não é (ao contrário do que geralmente se pensa) o facto de um utilizar O2 e o outro não!
Fermentação
Na fermentação, a molécula que recebe os electrões do NADH (ou FADH2) é um produto da mesma via metabólica que produziu o NADH (ou FADH2). Por exemplo, nos músculos, durante exercício físico intenso, o NADH produzido na glicólise transfere os seus electrões para o piruvato (uma molécula orgânica produzida também pela glicólise), dando origem a lactato.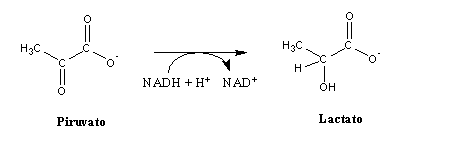
(A relação entre a descida do pH dos músculos durante a produção do lactato e a ocorrência de cãibras é discutida em pormenor nestes dois artigos). Esta é a fermentação láctica . Existem muitos outros tipos de fermentação em microorganismos, sendo o mais conhecido a fermentação alcoólica:
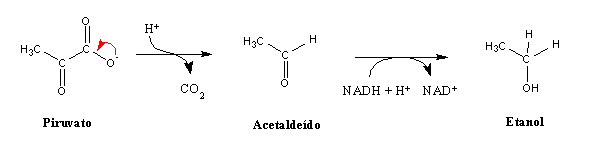
Respiração
Na respiração, a molécula que recebe os electrões do NADH (ou FADH2) não é um produto da mesma via metabólica que produziu o NADH (ou FADH2). Existem microorganismos que utilizam como aceitador de electrões SO42-, SeO42- ,NO3-, NO2-, NO, U6+ (urânio), Fe3+, H+, etc. Os mamíferos utilizam O2, e a sua respiração é por isso chamada respiração aeróbica. A respiração aeróbica ocorre na membrana interna da mitocôndria, que contém os complexos proteicos de transferência electrónica. Cada um destes complexos recebe electrões de uma molécula e transfere-os para outra molécula diferente, e o conjunto chama-se por isso cadeia transportadora de electrões: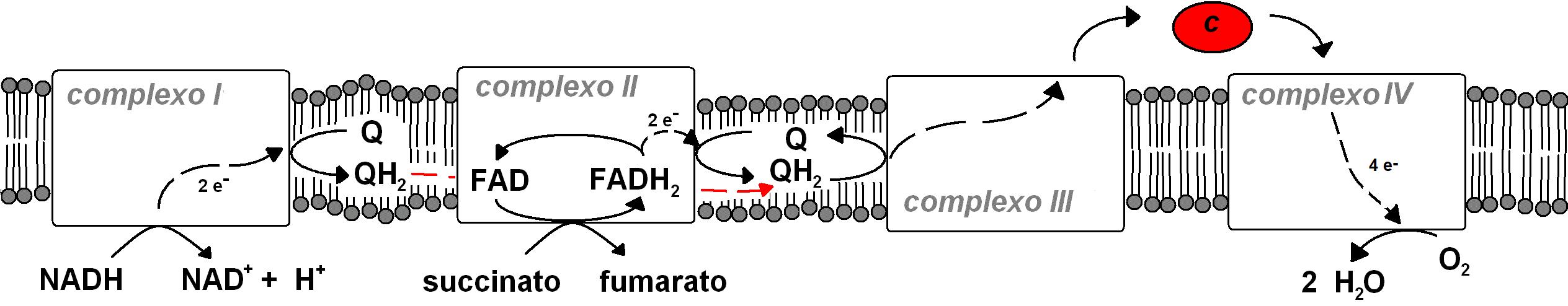
 Nos complexos I, III e IV a transferência electrónica liberta energia suficiente para transportar H+ da matriz mitocondrial para o espaço intermembranar. Isto provoca um aumento da concentração de H+ (e do potencial eléctrico) no espaço intermembranar, i.e. um maior potencial químico do H+ no espaço intermembranar do que na matriz. No entanto, quando se têm duas soluções de potencial químico diferente separadas por uma membrana, o soluto tem tendência para se deslocar do local onde o seu potencial químico é maior para o local em que o seu potencial químico é menor (o que, para uma substância sem carga eléctrica, é equivalente a mover-se dos locais de maior concentração para os de menor concentraçao).
Nos complexos I, III e IV a transferência electrónica liberta energia suficiente para transportar H+ da matriz mitocondrial para o espaço intermembranar. Isto provoca um aumento da concentração de H+ (e do potencial eléctrico) no espaço intermembranar, i.e. um maior potencial químico do H+ no espaço intermembranar do que na matriz. No entanto, quando se têm duas soluções de potencial químico diferente separadas por uma membrana, o soluto tem tendência para se deslocar do local onde o seu potencial químico é maior para o local em que o seu potencial químico é menor (o que, para uma substância sem carga eléctrica, é equivalente a mover-se dos locais de maior concentração para os de menor concentraçao).
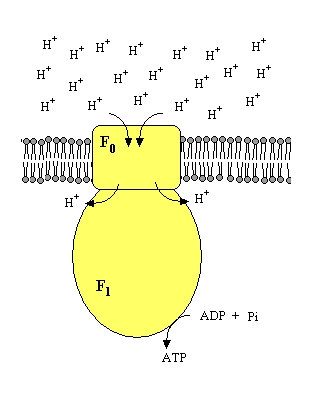
No entanto, como a membrana interna da mitocôndria é impermeável ao H+, em condições normais a única forma destes protões voltarem para a matriz é através de uma proteína especial: a ATP sintetase. Esta proteína é constituída por duas partes: um canal intermembranar de protões (F0) e uma porção voltada para a matriz mitocondrial (F1). A porção F1 é constituída por várias subunidades com diferentes funções, e usa a energia do movimento de protões de volta à matriz para sintetizar ATP a partir de ADP e Pi.
A quantidade de ATP produzida pela ATP sintetase está por isso relacionada com a diferença de concentração de H+ através da membrana. Uma vez que a oxidação do NADH provoca transferência de protões da matriz para o espaço intermembranar em 3 complexos (I, III e IV) ao passo que a oxidação do FADH2 só provoca essa transferência em dois complexos (III e IV) a quantidade de ATP produzida a partir do NADH é maior do que a produzida a partir do FADH2. São produzidos quase 3 ATP por NADH e quase 2 ATP por cada FADH2.
O NADH não consegue atravessar a membrana da mitocôndria. Existem por isso processos para transferir os electrões do NADH produzido no citoplasma durante a glicólise para a cadeia transportadora de electrões. Estes são:
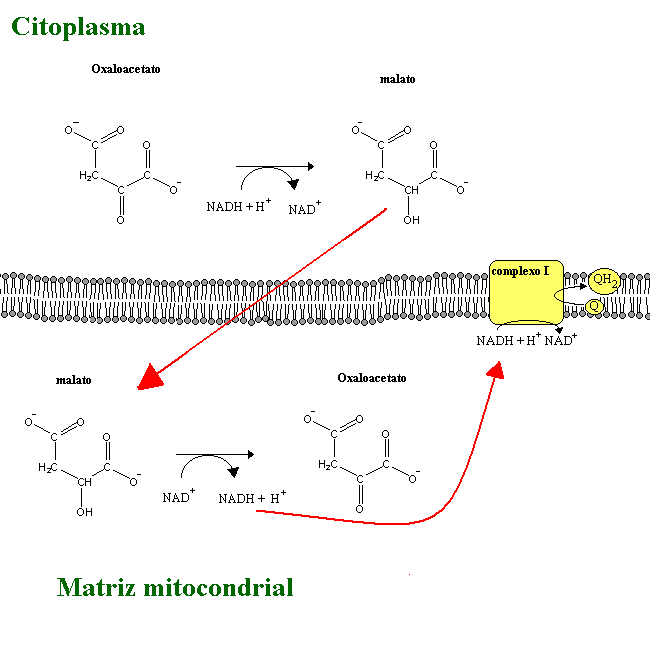
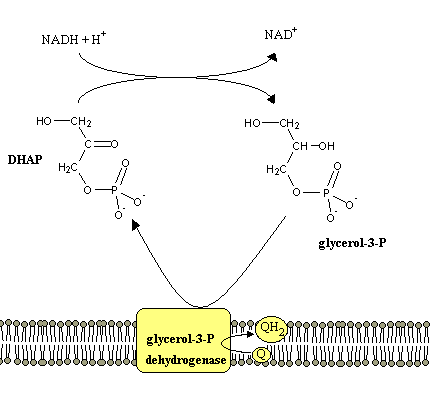
É possível ocorrer respiração mitocondrial sem produção de ATP: basta arranjar uma forma de fazer com que os protões regressem à matriz sem passarem pela ATP sintetase. Isto pode ser feito com ionóforos: moléculas lipossolúveis com capacidade de transportar iões. São produzidas p. ex. por plantas, para se defenderem de fungos parasitas. No tecido adiposo castanho, existe uma proteína (a termogenina) que funciona como canal de protões na membrana interna da mitocôndria: o regresso dos protões à matriz através dessa proteína em vez da ATP sintetase é responsável pela geração de calor característica deste tipo de tecido.
 |
Biochemistry,
by Donald Voet & Judith Voet Um excelente livro. Expõe a Bioquímica com referências constantes à química orgânica e à lógica bioquímica. A inspiração destas páginas.... Particularmente indicado a estudantes de Licenciaturas em Bioquímica, Ciências Farmacêuticas ou Química. |
 |
Biochemistry,
Stryer Um texto clássico, frequentemente actualizado e re-editado. |
 |
Textbook
of Biochemistry with Clinical Correlations, Thomas Devlin Aconselhado a estudantes de licenciaturas em Medicina, Enfermagem, etc. Imensos exemplos da aplicação da bioquímica a casos clínicos |
 |
Principles
of Biochemistry, Lehninger Um texto clássico, frequentemente actualizado e re-editado. |