Professor Associado, Universidade Fernando Pessoa
| Outras vias metabólicas: | |||
| Química Orgânica: |
Logo que entra na célula, a glucose é fosforilada a glucose-6-P pela enzima hexocinase:
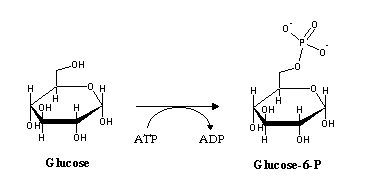
A membrana celular é impermeável à glucose-6-fosfato, que pode por isso ser acumulada na célula. A glucose-6-fosfato será utilizada na síntese do glicogénio (uma forma de armazenamento de glucose), na síntese de outros compostos de carbono na via das pentoses fosfato, ou degradada para produzir energia - glicólise.
Grandes quantidades de glucose-6-P dentro da célula provocam um aumento da pressão osmótica. Nessas condições a água terá tendência a entrar para dentro da célula, provocando um aumento do seu volume e eventual lise. Por isso, a glucose-6-P vai ser armazenada sob a forma de um polímero: o glicogénio. O glicogénio é um polissacarídeo pouco solúvel (e que portanto não provoca aumento da pressão osmótica), bastante ramificado e constituído exclusivamente por monómeros de glucose unidos entre si por ligações a-1,4 e a-1,6 (nas ramificações):
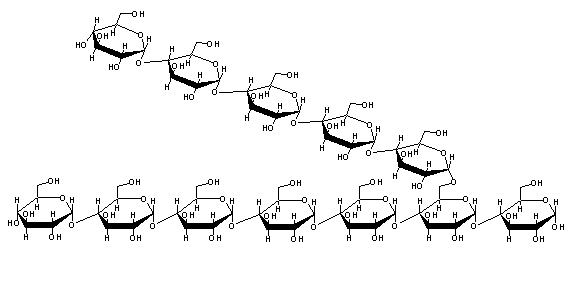
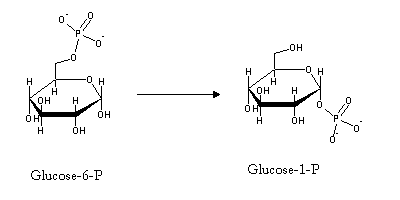
A adição de glucose-1-P ao carbono 4' de uma extremidade da cadeia de glicogénio não é uma reacção favorecida termodinamicamente em condições fisiológicas, uma vez que o potencial de transferência de fosfato das ligações C-O-P normais é bastante baixo. Por isso, a glucose-1-P vai ser activada, i.e., vai ser transformada numa espécie com alto potencial de transferência de fosfato. Isto é conseguido por reacção com uridina trifosfatafa (UTP, uma molécula análoga do ATP, mas com uridina no lugar da adenina).
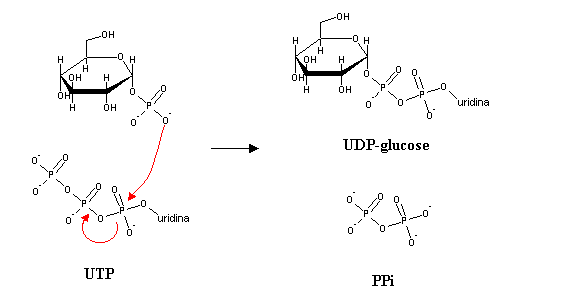
Esta reacção, só por si, não parece ser termodinamicamente favorável, pelo que se poderia pensar que não teria utilidade. No entanto, o pirofosfato (PPi) que se forma nesta reacção pode ser hidrolizado, numa reacção bastante exergónica. A eliminação do PPi empurra o equilíbrio no sentido de formação da UDP-glucose, ilustrando mais uma vez o princípio da utilização de uma reacção bastante exergónica para tornar espontânea uma outra reacção que de outra forma não seria favorecida termodinamicamente.
A UDP-glucose tem um elevado potencial de transferência de fosfato, o que lhe permite doar glucose à extremidade 4' de uma cadeia de glicogénio, numa reacção catalizada pela glicogénio sintase:
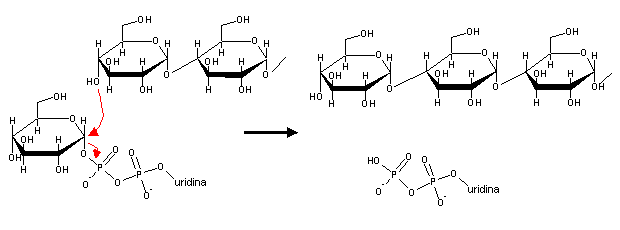
A glicogénio sintase só consegue adicionar glucose a cadeias de glicogénio pré-existentes, i.e., não é capaz de começar a síntese de uma nova molécula de glicogénio. A síntese do glicogénio é iniciada pela adição de uma molécula de glucose a um resíduo de tirosina de uma proteína denominada glicogenina.
As ramificações são realizadas por uma "enzima ramificadora". Esta actua sobre cadeias lineares de glicogénio com pelo menos 11 glucoses. A enzima ramificadora (amilo(1,4 -->1,6)-transglicosilase) transfere segmentos terminais de glicogénio de cerca de 7 resíduos de glucose para o grupo OH no carbono 6 de um resíduo de glucose (que pode estar na mesma ou noutra cadeia). As ramificações devem estar a pelo menos 4 resíduos de distância uma da outra.
O glicogénio é degradado pela acção conjunta de três enzimas:
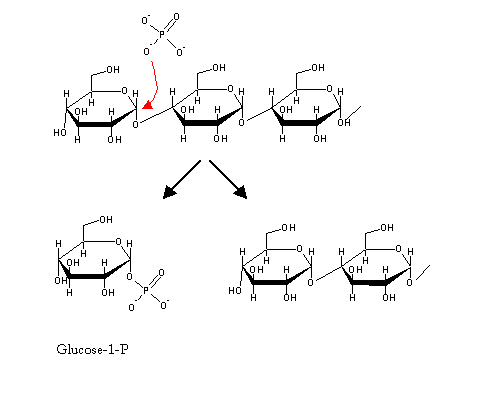
Uma molécula de glicogénio com ramos de apenas 4 glucoses (o que se denomina uma "dextrina-limite") não pode ser degradada apenas pela glicogénio fosforilase. Necessita da acção da enzima seguinte:
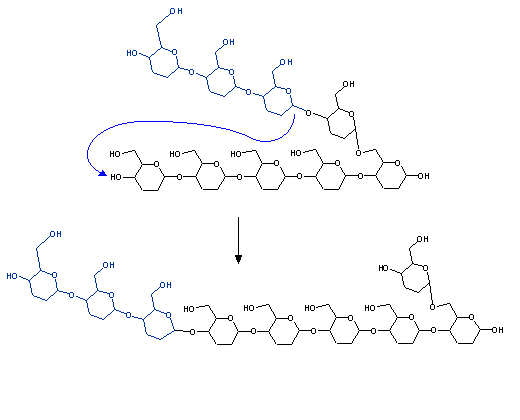
A glicogénio fosforilase é bastante mais rápida do que a enzima desramificadora, pelo que os ramos exteriores do glicogénio são degradados muito rapidamente no músculo em poucos segundos quando é necessária muita energia. A degradação do glicogénio para lá deste ponto exige a enzima desramificadora e é portanto mais lenta, o que explica em parte o facto do musculo só poder exercer a sua máxima força durante poucos segundos.
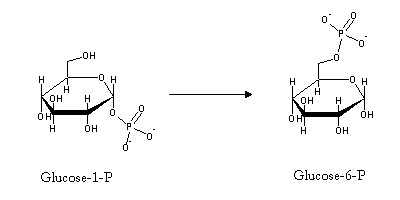
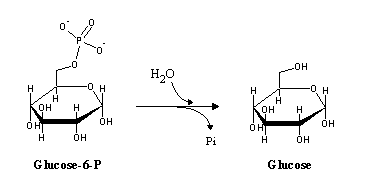
A glucose 6-fosfato pode então ser utilizada na glicólise. Ao contrário do músculo, o fígado (e em menor extensão, o rim) possui glucose-6-fosfatase, uma enzima hidrolítica que cataliza a desfosforilação da glucose 6-fosfato, o que lhe permite fornecer glucose ao resto do organismo:
 |
Biochemistry,
by Donald Voet & Judith Voet Um excelente livro. Expõe a Bioquímica com referências constantes à química orgânica e à lógica bioquímica. A inspiração destas páginas.... Particularmente indicado a estudantes de Licenciaturas em Bioquímica, Ciências Farmacêuticas ou Química. |
 |
Biochemistry,
Stryer Um texto clássico, frequentemente actualizado e re-editado. |
 |
Textbook
of Biochemistry with Clinical Correlations, Thomas Devlin Aconselhado a estudantes de licenciaturas em Medicina, Enfermagem, etc. Imensos exemplos da aplicação da bioquímica a casos clínicos |
 |
Principles
of Biochemistry, Lehninger Um texto clássico, frequentemente actualizado e re-editado. |