Professor Associado, Universidade Fernando Pessoa
| Outras vias metabólicas: | |||
| Química Orgânica: |
A maior parte da reserva energética do organismo encontra-se armazenada sob a forma de triacilglicéridos. Estes podem ser hidrolizados por lipases a glicerol e ácidos gordos:
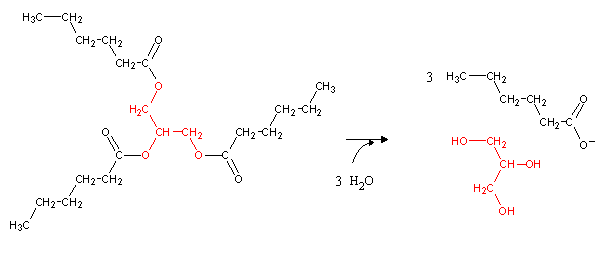
O glicerol pode seguir para a glicólise depois de oxidado a dihidroxiacetona fosfatada na face externa da membrana interna da mitocôndria. Os dois electrões libertados nesta oxidação são recebidos pela ubiquinona (Q), que os transfere para a cadeia transportadora de electrões.
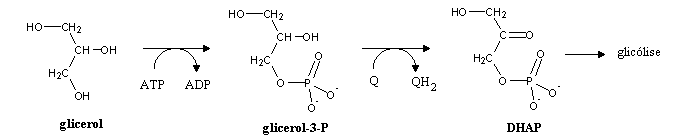
Os ácidos gordos terão um destino diferente: a β-oxidação, que ocorre na mitocôndria. Antes de entrarem na mitocôndria, os ácidos gordos são activados. A reacção de activação ocorre no citoplasma, e consiste na sua transformação em acil-CoA. Como sabemos do ciclo de Krebs, as ligações tioéster são muito energéticas: para a fazer, um ATP é hidrolizado a AMP (equivalente à hidrólise de 2 ATP em 2 ADP).
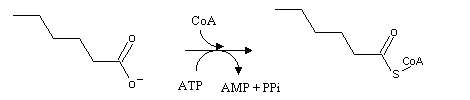
A membrana da mitocôndria é impermeável aos acil-CoA. Para entrarem na mitocôndria estes reagem com um aminoácido "especial", a carnitina, libertando a coenzima A. A carnitina esterificada é transportada para dentro da mitocôndria por um transportador específico. Dentro da mitocôndria, a carnitina transfere o grupo acilo para uma outra molécula de CoA. A carnitina livre volta então para o citoplasma através do transportador. Note que neste processo não existe transporte de CoA para dentro da mitocôndria: as reservas citoplasmática e mitocondrial de CoA não se misturam.
A b-oxidação dos ácidos gordos consiste num ciclo de 3 reacções sucessivas, idênticas à parte final do ciclo de Krebs: desidrogenação, hidratação da ligação dupla formada e oxidação do álcool a uma cetona:
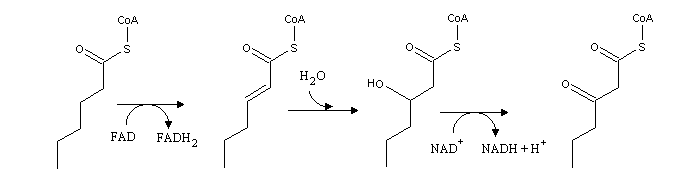
Por acção da enzima tiolase, liberta-se acetil-CoA, e um acil-CoA com menos dois carbonos que o acil-CoA original.
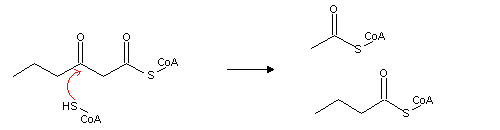
A repetição do ciclo permite a degradação total de um ácido gordo de cadeia par em acetil-CoA, que pode entrar no ciclo de Krebs, onde é completamente oxidado a CO2. É por isso impossível utilizar acetil-CoA para produzir oxaloacetato para (a partir deste), realizar a gluconeogénese.
Os ácidos gordos insaturados seguem um percurso semelhante, embora novas enzimas sejam necessárias para a oxidação na proximidade da ligação insaturada. No caso desta ligação se localizar num carbono ímpar, intervém a Δ3, Δ2-enoil-CoA isomerase. Esta enzima transfere a ligação dupla do carbono 3 para o carbono 2, permitindo a continuação da β-oxidação. Neste ciclo de β-oxidação não se forma FADH2.
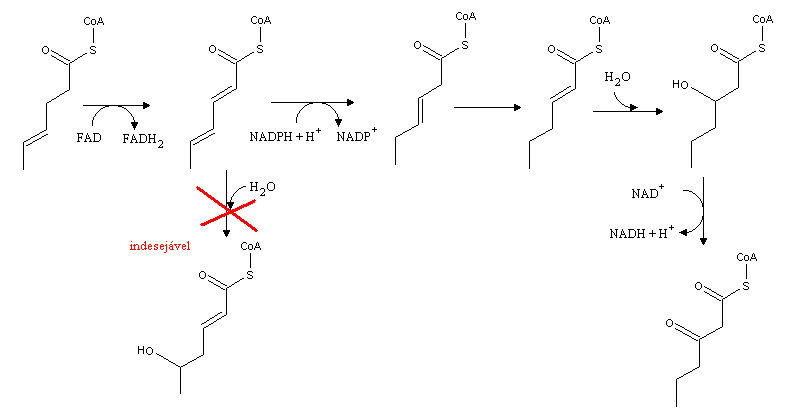
No caso da ligação dupla se localizar num carbono par, é necessária a intervenção da 2,4-dienoil-CoA reductase: a presença das ligações duplas conjugadas faz com que a reacção de hidratação tenha mais tendência a ocorrer no carbono 4 do que no carbono correcto (2). A 2,4-dienoil-CoA reductase transforma as ligações conjugadas Δ4, Δ2 numa única ligação dupla Δ3. Os electrões necessários para esta conversão provêm do NADPH. O processo continua seguidamente de forma análoga à oxidação de ácidos gordos insaturados em carbono ímpar.
Um ácido gordo de cadeia ímpar
dá origem, na última ronda do ciclo a acetil-CoA e
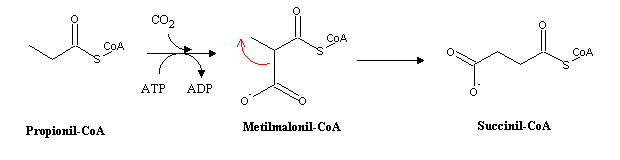
propionil-CoA. Para que este possa ser utilizado pelo ciclo de
Krebs, é necessário adicionar-lhe um átomo de carbono, o que
é feito por carboxilação. O metilmalonil
assim formado é então rearranjado a succinil-CoA, numa
reacção assistida pela cobalamina (a vitamina B12). O succinil-CoA, além de ser um intermediário no ciclo de
Krebs, é um precursor do hemo. Uma deficiência em vitamina B12
resulta por isso na dificuldade de sintetizar hemo, i.e., no
desenvolvimento de anemia perniciosa. Esta
doença é o resultado da dificuldade de sequestrar cobalamina a
nível do estômago, e surge em indivíduos predispostos em idade
avançada. Antes dos modernos meios de produção de cobalamina,
o tratamento consistia na ingestão diária de quantidades
razoáveis de fígado cru, que é bastante rico nesta vitamina. O
aparecimento da doença quase só em indivíduos idosos é uma
consequência do facto de termos no fígado uma reserva de B12
suficiente para cerca de 3-5 anos, pelo que deficiências na sua
absorção têm um efeito muito retardado. O succinil-CoA é oxidado pelo ciclo de Krebs a
malato, que depois de passar para o citoplasma pode ser utilizado
na gluconeogénese. No citoplasma
pode também ser descarboxilado a piruvato pela enzima
málica, com produção simultânea de NADPH: O piruvato pode entrar na mitocôndria, e ser completamente
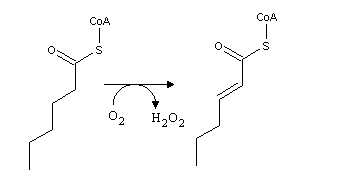
oxidado a CO2 pelo ciclo de Krebs. Os peroxissomas são pequenos organelos onde decorre a b-oxidação de ácidos gordos de cadeia
longa, de forma a facilitar a sua degradação subsequente pela
mitocôndria. As principais diferenças entre os dois processos
são: Uma grande quantidade do acetil-CoA produzido pela b-oxidação dos ácidos gordos nas
mitocôndrias do fígado é convertida em acetoacetato
e b-hidroxibutirato
(também denominados corpos cetónicos). Estes
compostos podem ser usados pelo coração e pelos músculos
esqueléticos para produzir energia. O cérebro, que normalmente
depende da glucose como fonte de energia, pode também utilizar
corpos cetónicos durante um jejum prolongado (maior do que
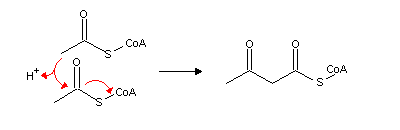
2-3-dias). A síntese de corpos cetónicos começa pela
condensação de duas moléculas de acetil-CoA, para formar
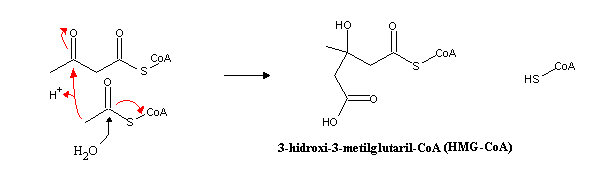
acetoacetil-CoA: A condensação de outra molécula de acetil-CoA
produz 3-hidroxi-3-metil-glutaril-CoA (HMG-CoA). Esta reacção
é idêntica, no seu mecanismo, à condensação
do oxaloacetato com o acetil-CoA para formar citrato, que
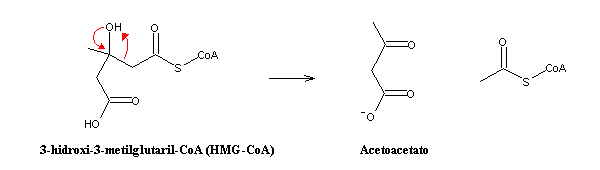
ocorre no ciclo de Krebs. O HMG-CoA é então degradado a acetoacetato e
acetil-CoA: O acetoacetato assim produzido passa para a corrente sanguínea
e é distribuído pelos tecidos. Uma vez absorvido, reage na
mitocôndria com o succinil-CoA, produzindo succinato e acetoacetil-CoA, que
pode ser clivado em duas moléculas de acetil-CoA. Em situações de abundância de acetil-CoA, o fígado e o
tecido adiposo sintetizam ácidos gordos. O processo de síntese
apresenta bastantes semelhanças com o inverso da b-oxidação, mas também tem diferenças
importantes: A síntese de ácidos gordos é feita a partir de acetil-CoA.
No entanto, o processo é endergónico, pelo que o acetil-CoA
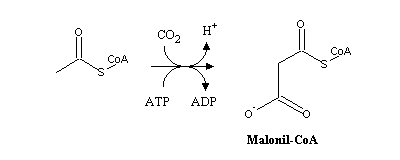
deve ser previamente activado. Este é portanto
carboxilado pela acetil-CoA carboxilase, uma enzima que tal como
as outras carboxilases (p.ex., do
piruvato ou do propionil-CoA) possui
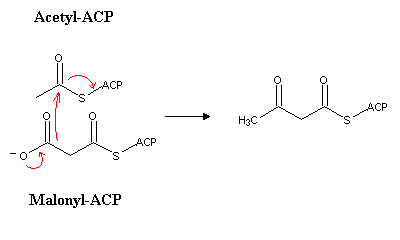
biotina: O malonil é então transferido para a proteína
transportadora de acilos (ACP), dando a origem a malonil-ACP.
Este será então condensado com acetil-ACP (sintetizado de forma
semelhante a partir de acetil-CoA). Em animais, todos os passos da síntese do ácido palmítico
(o ácido gordo saturado com 16 carbonos) são catalizados pela
sintase dos ácidos-gordos, uma enzima bastante grande que leva a
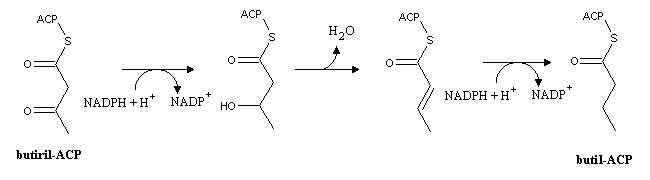
cabo todas as reacções seguintes desta via. O butiril-ACP
produzido na primeira reacção vai ser transformado em
butil-ACP. A sequência de reacções é o inverso da que ocorre
na b-oxidação, i.e., redução,
desidratação e hidrogenação: O butil-ACP pode então condensar com outra
molécula de malonil-ACP. O ciclo repete-se sete vezes, até se
formar palmitoil-ACP, que por hidrólise produz ácido
palmítico. A estequiometria da síntese do ácido palmítico é
portanto: Acetil-CoA + 7 Malonil-CoA + 14 NADPH + 7 H+
---> palmitato + 7 CO2 + 14 NADP+ + 8
CoA + 6 H2O Ácidos gordos insaturados ou de cadeia mais
longa são produzidos a partir do ácido palmítico por acção
de elongases e desaturases. Note que a síntese de ácidos gordos ocorre no
citoplasma, ao passo a a síntese de acetil-CoA ocorre na
mitocôndria. É por isso necessário transportar acetil-CoA para
o citoplasma. Isto é feito pelo sistema de transporte dos
ácidos tricarboxílicos, também chamado ciclo do
citrato: o citrato formado na mitocôndria por condensação do acetil-CoA com
oxaloacetato difunde-se para o citoplasma, onde é clivado
pela citrato-liase em acetil-CoA e oxaloacetato, que é depois
reduzido a malato, que se pode difundir de volta para a
mitocôndria. Por acção da enzima málica,
o malato também pode ser usado para produzir parte do NADPH
necessário para a síntese dos ácidos gordos. O restante NADPH
deve ser produzido pela via das
pentoses-fosfato. Um excelente livro. Expõe a Bioquímica com referências constantes à química orgânica e à lógica bioquímica. A inspiração destas páginas.... Particularmente indicado a estudantes de Licenciaturas em Bioquímica, Ciências Farmacêuticas ou Química. Um texto clássico, frequentemente actualizado e re-editado. Aconselhado a estudantes de licenciaturas em Medicina, Enfermagem, etc. Imensos exemplos da aplicação da bioquímica a casos clínicos
Um texto clássico, frequentemente actualizado e re-editado. 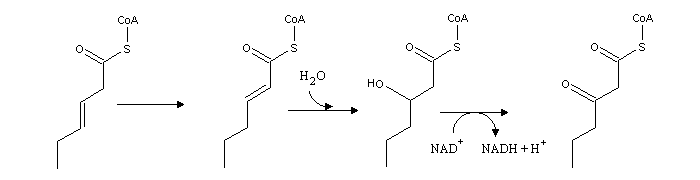
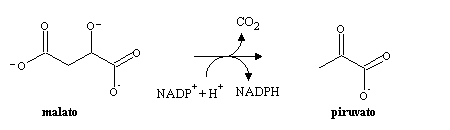
Degradação peroxissomal de ácidos gordos
Síntese de corpos cetónicos (Cetogénese)
Síntese de ácidos gordos
Bibliografia

Biochemistry,
by Donald Voet & Judith Voet

Biochemistry,
Stryer

Textbook
of Biochemistry with Clinical Correlations, Thomas Devlin

Principles
of Biochemistry, Lehninger